精选
精选
抗生素的突破:革命性的中国研究为超级细菌击败药物铺平了道路
诸平

据威利(WILEY)出版公司2024年4月23日提供的消息,抗生素的突破:革命性的中国研究为超级细菌击败药物铺平了道路(Antibiotic Breakthrough: Revolutionary Chinese Study Paves Way for Superbug Defeating Drugs)。中国研究小组开发的一种新方法,引入了基于含氟脂链的蛋白质构建块的抗生素(Antibiotics),以对抗多重耐药细菌。该方法利用脂蛋白的独特特性,通过合成含氟脂肽,在小鼠模型中已被证明对耐甲氧西林金黄色葡萄球菌(methicillin-resistant Staphylococcus aureus简称MRSA)有效,为治疗耐药细菌感染而不诱导耐药性提供了一条有希望的途径。
新的研究表明,含氟脂肽(fluorous lipopetides)是一种非常有效的抗生素。
细菌感染对多种药物具有耐药性,现有抗生素无法治疗,这是一项重大的全球性挑战。来自中国的一个研究小组2024年2月23日在德国《应用化学国际版》(Angewandte Chemie International Edition)杂志上提出了一种新的策略,用于制造旨在对抗这些耐药细菌的创新抗生素。这种方法利用蛋白质成分与含氟脂链(fluorous lipid chains)结合来开发药物。原文详见:Dr. Jingjing Hu, Nan Liu, Dr. Qianqian Fan, Yunqing Gu, Sijia Chen, Dr. Fang Zhu, Prof. Yiyun Cheng. A Fluorous Peptide Amphiphile with Potent Antimicrobial Activity for the Treatment of MRSA-induced Sepsis and Chronic Wound Infection. Angewandte Chemie International Edition,2024. DOI: 10.1002/anie.202403140. First published: 23 February 2024. https://doi.org/10.1002/anie.202403140
抗生素(Antibiotics)的处方往往过于容易。在许多国家,它们在没有处方的情况下分发,并在工厂化养殖中进行管理:预防性地预防感染并提高绩效。因此,对储备抗生素的耐药性也日益上升。开发创新的替代方案至关重要。
从微生物中学习(Learning from Microbes)
我们可以从微生物身上学到一些东西。脂蛋白(Lipoproteins)是一种带有脂肪酸链的小蛋白质分子,被细菌广泛用于对抗微生物竞争对手。许多脂蛋白已经被批准作为药物使用。活性脂蛋白的共同因素包括带正电荷和两亲性结构(amphiphilic structure),这意味着它们有排斥脂肪的部分,也有排斥水的部分。这使它们能够与细菌膜结合并穿透它们进入内部。
中国上海华东师范大学程义云(Yiyun Cheng)教授领导的一个研究小组旨在通过用氟原子取代脂质链中的氢原子来放大这种效应。这使得脂链同时具有疏水性(hydrophobic)和疏脂性(lipophobic)。它们特别低的表面能加强了它们与细胞膜的结合,而它们的疏脂性破坏了细胞膜的凝聚力。
含氟脂肽的合成与筛选(Synthesis and Screening of Fluorous Lipopeptides)
该团队从氟化烃(fluorinated hydrocarbons)和肽链(peptide chains)合成了含氟脂肽的光谱/物质库(spectrum / substance library)。为了连接这两个片段,他们使用了氨基酸半胱氨酸(amino acid cysteine),它通过二硫桥(disulfide bridge)将它们连接在一起。研究人员通过测试这些分子对耐甲氧西林金黄色葡萄球菌(MRSA)的活性来筛选这些分子。耐甲氧西林金黄色葡萄球菌是一种广泛存在的、高度危险的细菌菌株,几乎对所有抗生素都有抗药性。他们发现最有效的化合物是R6F,这是一种含氟的脂肽(fluorous lipopeptide),由6个精氨酸单元(arginine units)和8个碳原子和13个氟原子组成的脂链组成。为了提高生物相容性(biocompatibility),R6F被包裹在磷脂纳米颗粒(phospholipid nanoparticles)中。
在小鼠模型中,R6F纳米颗粒被证明对MRSA引起的败血症和慢性伤口感染非常有效,未见毒副作用。纳米颗粒似乎从几个方面攻击细菌:它们抑制重要细胞壁成分的合成,促进细胞壁坍塌;它们还能刺穿细胞膜,破坏细胞膜的稳定;扰乱呼吸链和新陈代谢;增加氧化应激,同时破坏细菌的抗氧化防御系统。综合起来,这些作用杀死了其他细菌和MRSA。似乎没有产生耐药性。
这些见解为开发高效的氟肽药物治疗多重耐药细菌提供了起点。
本研究得到了中国国家重点研发计划(National Key Research and Development Program of China)、中国国家自然科学基金(National Natural Science Foundation of China)以及中国上海市科学技术委员会(Science and Technology Commission of Shanghai Municipality)的资助。
上述介绍,仅供参考。欲了解更多信息,敬请注意浏览原文或者相关报道。
A fluorous peptide amphiphile R6F shows high antibacterial effect via permeabilizing bacteria membrane, disrupting the respiratory reaction and antioxidant defense system of bacteria, and destroying the peptidoglycan in cell wall. R6F was further prepared into lipid nanoparticles and efficiently treated the MRSA-induced sepsis and wound infections with minimal side effects.
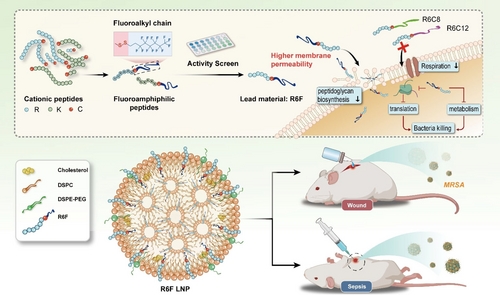
The rising prevalence of global antibiotic resistance evokes the urgent need for novel antimicrobial candidates. Cationic lipopeptides have attracted much attention due to their strong antimicrobial activity, broad-spectrum and low resistance tendency. Herein, a library of fluoro-lipopeptide amphiphiles was synthesized by tagging a series of cationic oligopeptides with a fluoroalkyl tail via a disulfide spacer. Among the lipopeptide candidates, R6F bearing six arginine moieties and a fluorous tag shows the highest antibacterial activity, and it exhibits an interesting fluorine effect as compared to the non-fluorinated lipopeptides. The high antibacterial activity of R6F is attributed to its excellent bacterial membrane permeability, which further disrupts the respiratory chain redox stress and cell wall biosynthesis of the bacteria. By co-assembling with lipid nanoparticles, R6F showed high therapeutic efficacy and minimal adverse effects in the treatment of MRSA-induced sepsis and chronic wound infection. This work provides a novel strategy to design highly potent antibacterial peptide amphiphiles for the treatment of drug-resistant bacterial infections.
转载本文请联系原作者获取授权,同时请注明本文来自诸平科学网博客。
链接地址:https://wap.sciencenet.cn/blog-212210-1431390.html?mobile=1
收藏